脐带血来源CAR-NK细胞:一种更具应用前景的异体抗肿瘤免疫细胞
近日,美国安德森癌症中心的研究人员对脐带血来源的NK细胞进行了基因改造,探讨了其在抗肿瘤方面的作用和安全性问题,相关研究成果发表在Nature杂志子刊《Leukemia》上。
嵌合抗原受体(Chimeric antigen receptors,CARs)基因修饰自体T细胞已在白血病和淋巴瘤的特异性治疗中显示出较好的临床疗效。但是同种异体CAR-T细胞应用于治疗存在较大的移植物抗宿主病(GVHD)风险。自然杀伤(NK)细胞对靶细胞的识别和杀伤不依赖于抗原特异性,不会引起GVHD。脐带血(Cord blood,CB)为同种异体NK细胞免疫治疗提供了一种极具吸引力的细胞来源。
来自美国安德森癌症中心的研究人员利用逆转录病毒感染CB来源的NK细胞,使其表达CAR-CD19、IL-15和可诱导性caspase-9自杀基因(iC9),该基因修饰后的CB-NK(iC9/CAR.19/IL-15 CB-NK)细胞可以高效杀伤CD19阳性的细胞系(图1)和原代白血病细胞(图2),且可以显著延长异种移植Raji淋巴瘤小鼠的生存期(图3)。尤为重要的是,该iC9/CAR.19/IL-15 CB-NK细胞可以通过药物激活iC9自杀基因,从而在必要时清除该基因修饰NK细胞(图4)。
总之,基因修饰CB来源的NK细胞为同种异体免疫治疗提供了一种易制备、疗效惊人且安全性高的途径。
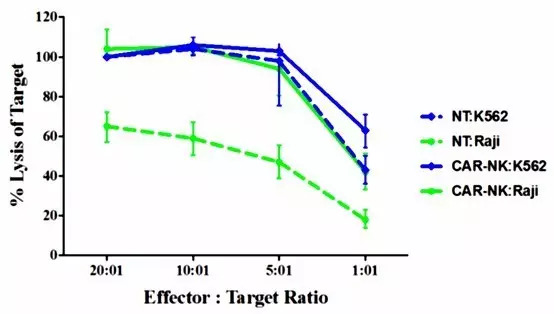
图1 未感染CB-NK(NT)细胞和基因修饰后的CB-NK(CAR-NK)细胞对CD19+ Raji细胞的杀伤效率
注:CD19- K562细胞系作为阳性对照
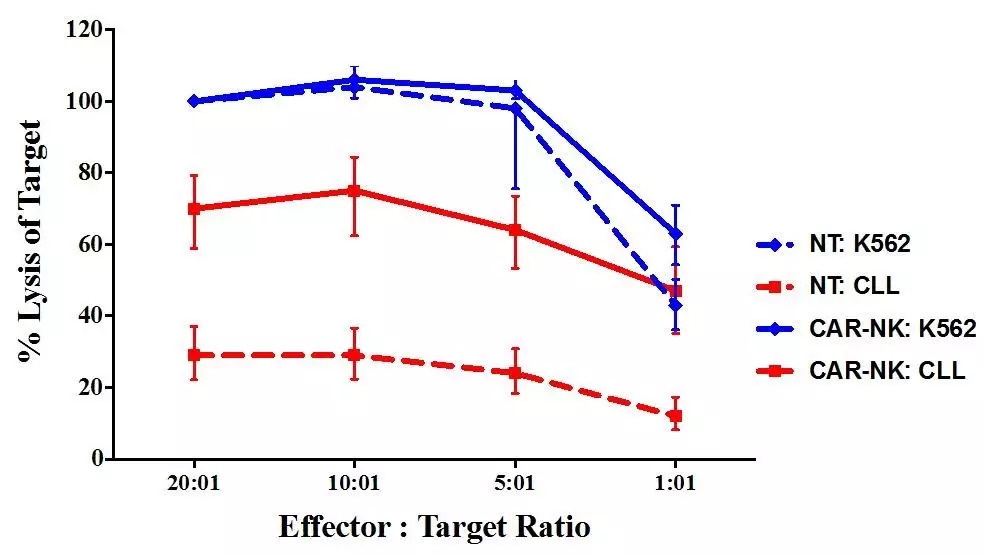
图2 未感染CB-NK(NT)细胞和基因修饰后的CB-NK(CAR-NK)细胞对原代白血病细胞CLL细胞系的杀伤效率
注:CD19- K562细胞系作为阳性对照
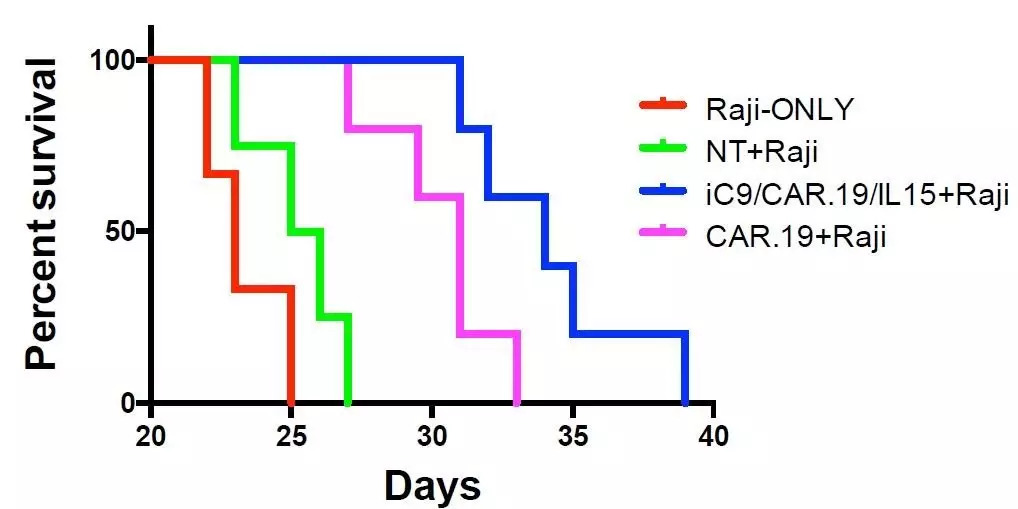
图3未感染CB-NK(NT)细胞、基因修饰后的CB-NK(iC9/CAR.19/IL-15)细胞及
CAR-19基因修饰的CB-NK(CAR.19)细胞治疗Raji细胞移植瘤小鼠模型的生存期对比
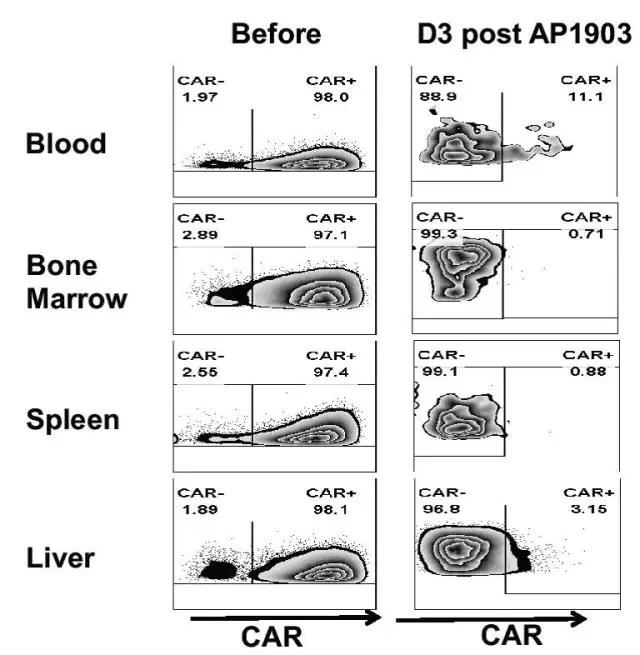
图4 药物诱导处理前后小鼠体内CAR-NK细胞比例的流式检测结果
 关注公司微信公众号
关注公司微信公众号 地址:深圳市龙华新区宝能科技园